FDA erteilt Zulassung für Krebsimmuntherapeutikum TECENTRIQ (Atezolizumab) von Roche für Patienten mit bestimmter Form von metastasierendem Lungenkrebs
2016-10-19
- Erstes und einziges von der FDA zugelassenes Anti-PD-L1-Krebsimmuntherapeutikum für metastasierenden nicht-kleinzelligen Lungenkrebs (NSCLC)
- Zulassung stützt sich auf Überlebensvorteil mit TECENTRIQ, verglichen mit Docetaxel-Chemotherapie, unabhängig vom PD-L1-Status
Roche (SIX: RO, ROG; OTCQX: RHHBY) gab heute bekannt, dass die amerikanische Zulassungsbehörde FDA (Food and Drug Administration) die Zulassung für TECENTRIQ® (atezolizumab) zur Behandlung von Patienten mit metastasierendem nicht-kleinzelligem Lungenkrebs (NSCLC) erteilt hat, deren Erkrankung während oder nach platinhaltiger Chemotherapie oder, bei Tumoren mit EGFR- oder ALK-Genmutationen unter geeigneter zielgerichteter Therapie, weiter fortgeschritten ist. Diese Zulassung stützt sich auf die Resultate der randomisierten Phase-III-Studie OAK und der Phase-II-Studie POPLAR. Wie die grössere OAK-Studie zeigte, führte TECENTRIQ dazu, dass die Patienten in der Gesamtpopulation der Studie 13,8 Monate (Median) überlebten und damit 4,2 Monate länger als die mit Docetaxel-Chemotherapie behandelten Patienten (medianes Gesamtüberleben [OS]: 13,8 vs. 9,6 Monate; HR=0,74, 95%-KI: 0,6-0,87). Die Studie umfasste Patienten unabhängig von ihrem PD-L1-Status mit plattenepithelialen und nicht-plattenepithelialen Formen von Lungenkrebs.
„TECENTRIQ ist eine neue Behandlungsoption, unter der Patienten mit dieser Form von vorbehandeltem metastasierendem Lungenkrebs länger leben als unter Chemotherapie, und zwar auch Patienten mit niedriger oder keiner gemessenen Expression des PD-L1-Proteins“, so Sandra Horning, Chief Medical Officer und Leiterin der globalen Produktentwicklung von Roche. „TECENTRIQ ist das erste und einzige zugelassene Krebsimmuntherapeutikum, das gezielt gegen das Protein PD-L1 gerichtet ist, was wahrscheinlich eine wichtige Rolle bei der Wirkung des Medikaments spielt.“
Das Entwicklungsprogramm für TECENTRIQ umfasst mehr als 15 klinische Studien bei Lungenkrebs, darunter sieben Phase-III-Studien bei nicht vorbehandeltem Lungenkrebs (Erstlinientherapie). Diese Studien prüfen die Anwendung von TECENTRIQ allein oder in Kombination mit anderen Medikamenten.
Über die OAK-Studie
Bei der OAK-Studie handelt es sich um eine weltweite, multizentrische, offene, randomisierte und kontrollierte Phase-III-Studie zur Beurteilung der Wirksamkeit und Sicherheit von TECENTRIQ verglichen mit Docetaxel bei 1225 Patienten mit lokal fortgeschrittenem oder metastasierendem NSCLC, deren Erkrankung nach oder während einer vorherigen platinhaltigen Chemotherapie fortgeschritten war. Die primäre Analyse umfasste die ersten 850 randomisierten Patienten. Patienten mit plattenepithelialem und nicht-plattenepithelialem Lungenkrebs wurden im Verhältnis 1:1 für die Behandlung mit TECENTRIQ intravenös in der Dosierung von 1200 mg alle 3 Wochen oder Docetaxel intravenös in der Dosierung von 75 mg/m² alle 3 Wochen randomisiert. Koprimäre Endpunkte waren das Gesamtüberleben (OS) bei allen randomisierten Patienten (ITT-Population) und in einer PD-L1-selektierten Untergruppe der primären Analysepopulation.
Über die POPLAR-Studie
Bei POPLAR handelt es sich um eine multizentrische, offene, randomisierte Phase-II-Studie zur Beurteilung der Wirksamkeit und Sicherheit von TECENTRIQ verglichen mit Chemotherapie (Docetaxel) bei Patienten mit vorbehandeltem, wiederkehrendem, lokal fortgeschrittenem oder metastasierendem nicht-kleinzelligem Lungenkrebs (NSCLC). Primärer Endpunkt war das Gesamtüberleben (OS). Sekundäre Endpunkte waren das progressionsfreie Überleben (PFS), die objektive Ansprechrate (ORR) und die Sicherheit.
Die Wirksamkeitsdaten der OAK- und der POPLAR-Studie, die diese Zulassung stützen, werden im Folgenden zusammengefasst.
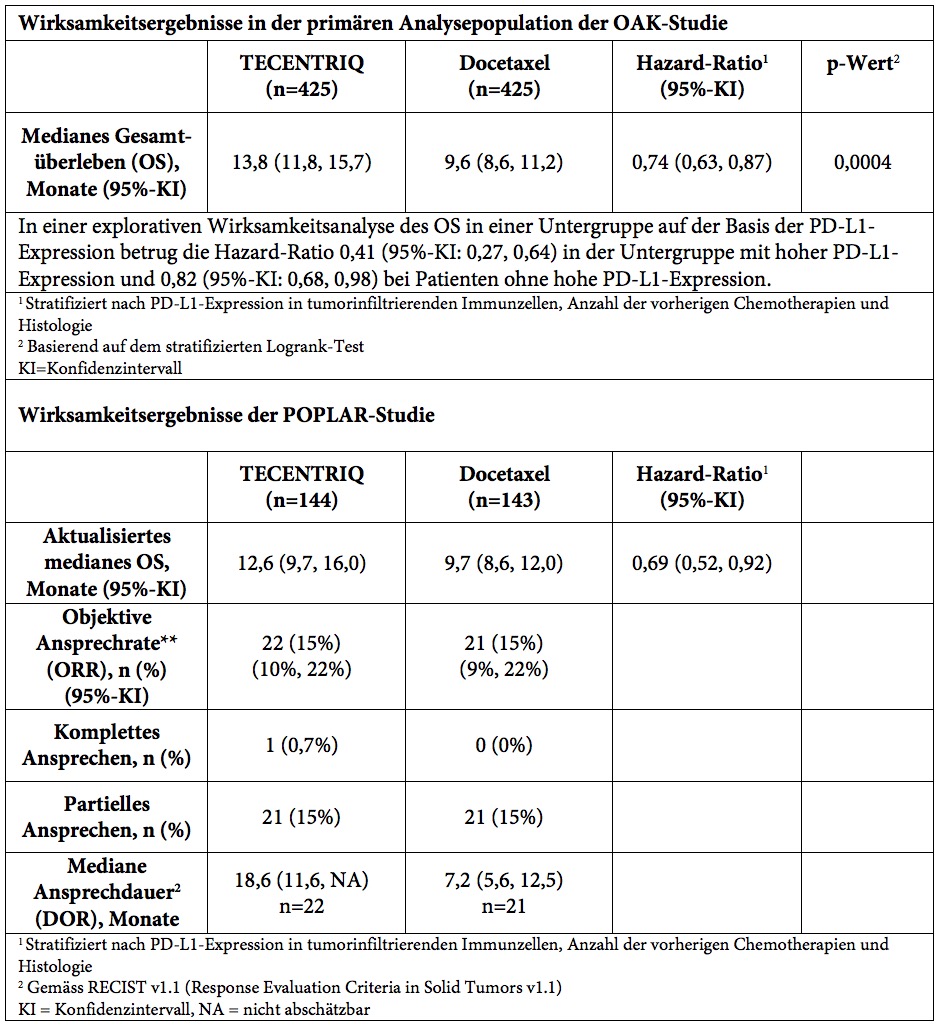
Die häufigsten Nebenwirkungen (≥ 20%) bei Patienten mit metastasierendem nicht-kleinzelligem Lungenkrebs waren Müdigkeit, verminderter Appetit, Dyspnoe (Kurzatmigkeit), Husten, Übelkeit, Muskel-Skelett-Schmerzen und Verstopfung. Bei neun Patienten (6,3%), die mit TECENTRIQ behandelt wurden, kam es zu Lungenembolie (2), Pneumonie (2), Pneumothorax, Ulkusblutung (blutendes Geschwür), Kachexie (Auszehrung) infolge von Dysphagie (Schluckstörung), Herzinfarkt oder Dickdarmperforation mit Todesfolge. Bei 6 der 142 Patienten (4 Prozent) wurde TECENTRIQ wegen unerwünschter Reaktionen abgesetzt.
Über nicht-kleinzelligen Lungenkrebs
Lungenkrebs ist weltweit die häufigste Krebstodesursache. Jedes Jahr sterben 1,59 Millionen Menschen an der Erkrankung. Das sind weltweit mehr als 4350 Todesfälle jeden Tag. Lungenkrebs kann grob in zwei Hauptformen eingeteilt werden, und zwar nicht-kleinzelligen (NSCLC) und kleinzelligen Lungenkrebs. Das NSCLC ist die häufigste Form der Erkrankung und für rund 85% aller Lungenkrebsfälle verantwortlich.
Über TECENTRIQ (Atezolizumab)
TECENTRIQ ist ein monoklonaler Antikörper, der zielgerichtet an das Protein PD-L1 (programmed death ligand-1, programmierter Zelltod-Ligand 1) bindet, das auf Tumorzellen und tumorinfiltrierenden Immunzellen exprimiert wird. PD-L1 interagiert mit den Proteinen PD-1 und B7.1 auf der Oberfläche von T-Zellen und führt dadurch zur Hemmung der T-Zellen. TECENTRIQ kann diese Wechselwirkung blockieren und so die T-Zellen wieder aktivieren und deren Fähigkeit zur Erkennung und Bekämpfung von Tumorzellen wieder herstellen. TECENTRIQ ist zurzeit nur in den USA zugelassen.
Über Roche in der Krebsimmuntherapie
Roche entwickelt seit über 50 Jahren Medikamente, um neue Behandlungsmassstäbe in der Onkologie zu setzen. Heute investieren wir mehr als je zuvor in unser Bestreben, innovative Behandlungsmöglichkeiten zu entwickeln, die das Immunsystem von Patienten bei der Krebsbekämpfung unterstützen.
Über personalisierte Krebsimmuntherapie (PCI)
Das Ziel der personalisierten Krebsimmuntherapie (PCI) sind Behandlungsmöglichkeiten, die auf die spezifische Immunbiologie des Tumors jedes einzelnen Patienten zugeschnitten sind. Darauf basieren Therapiestrategien, die möglichst vielen Patienten die Chance auf einen hohen Nutzen bieten. Im Falle von TECENTRIQ wird mit dem Biomarker PD-L1 die PD-L1-Expression auf Tumorzellen und tumorinfiltrierenden Immunzellen gemessen und untersucht, wie diese mit dem klinischen Nutzen der Monotherapie oder Kombinationstherapie bei einem breiten Spektrum von Krebsarten zusammenhängt. Das Forschungs- und Entwicklungsprogramm von Roche zur personalisierten Krebsimmuntherapie umfasst mehr als 20 Prüfkandidaten, von denen zehn bereits in klinischen Studien getestet werden.
Die personalisierte Krebsimmuntherapie ist ein wesentliches Element des breiteren Engagements von Roche für die personalisierte Medizin. Unter dem folgenden Link erfahren Sie mehr über die Strategie von Roche in der Krebsimmuntherapie:
http://www.roche.com/research_and_development/what_we_are_working_on/oncology/cancer-immunotherapy.htm
Über Roche
Roche ist ein globales Unternehmen mit Vorreiterrolle in der Erforschung und Entwicklung von Medikamenten und Diagnostika und ist darauf fokussiert, Menschen durch wissenschaftlichen Fortschritt ein besseres, längeres Leben zu ermöglichen.
Roche ist das grösste Biotech-Unternehmen weltweit mit differenzierten Medikamenten für die Onkologie, Immunologie, Infektionskrankheiten, Augenheilkunde und Erkrankungen des Zentralnervensystems. Roche ist auch der bedeutendste Anbieter von In-vitro-Diagnostika und gewebebasierten Krebstests und ein Pionier im Diabetesmanagement. Dank der Kombination von Pharma und Diagnostika unter einem Dach ist Roche führend in der personalisierten Medizin – einer Strategie mit dem Ziel, jedem Patienten die bestmögliche Behandlung zukommen zu lassen.
Seit der Gründung im Jahr 1896 erforscht Roche bessere Wege, um Krankheiten zu verhindern, zu erkennen und zu behandeln und leistet einen nachhaltigen Beitrag zur gesellschaftlichen Entwicklung. Auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation stehen heute 29 von Roche entwickelte Medikamente, darunter lebensrettende Antibiotika, Malariamittel und Krebsmedikamente. Ausgezeichnet wurde Roche zudem bereits das achte Jahr in Folge als das nachhaltigste Unternehmen innerhalb der Pharma-, Biotechnologie- und Life-Sciences-Branche im Dow Jones Sustainability Index.
Die Roche-Gruppe mit Hauptsitz in Basel, Schweiz ist in über 100 Ländern tätig und beschäftigte 2015 weltweit über 91 700 Mitarbeitende. Im Jahr 2015 investierte Roche CHF 9,3 Milliarden in Forschung und Entwicklung und erzielte einen Umsatz von CHF 48,1 Milliarden. Genentech in den USA gehört vollständig zur Roche-Gruppe. Roche ist Mehrheitsaktionär von Chugai Pharmaceutical, Japan. Weitere Informationen finden Sie unter www.roche.com.
Alle erwähnten Markennamen sind gesetzlich geschützt.
additional materials
Media
Media releases
stay updated
get the latest news and updates to your inbox.